1、研究意義與前景
層析法是利用混合物中各組分物理化學(xué)性質(zhì)的差異(如吸附力、分子形狀及大小、分子親和力、分配系數(shù)等),使各組分在兩相(一相為固定的,稱為固定相;另一相流過固定相,稱為流動相)中的分布程度不同,從而使各組分以不同的速度移動而達(dá)到分離的目的。【1】
紙層析法(paper chromatography)是生物化學(xué)上分離、鑒定氨基酸混合物的常用技術(shù),可用于蛋白質(zhì)的氨基酸成分的定性鑒定和定量測定;也是定性或定量測定多肽、核酸堿基、糖、有機(jī)酸、維生素、抗菌素等物質(zhì)的一種分離分析工具。紙層析法是用濾紙作為惰性支持物的分配層析法,其中濾紙纖維素上吸附的水是固定相,展層用的有機(jī)溶溶劑是流動相。【2】
分配層析法 分配色譜系色譜法之一種,利用固定相與流動相之間對待分離組分溶解度的差異來實(shí)現(xiàn)分離。分配色譜的固定相一般為液相的溶劑,依靠圖布、鍵合、吸附等手段分布于色譜柱或者擔(dān)體表面。分配色譜過程本質(zhì)上是組分分子在固定相和流動相之間不斷達(dá)到溶解平衡的過程。【3】
2、實(shí)驗?zāi)康?nbsp;
(1)掌握分配層析的原理,學(xué)習(xí)氨基酸紙層析法的操作技術(shù)(包括點(diǎn)樣、平衡、展層、顯色、鑒定及定量)
(2)學(xué)習(xí)未知樣品的氨基酸成分(水解、層析及鑒定)分析的方法。
3、實(shí)驗原理
層析法也稱色譜法,是1906年俄*植物學(xué)家Michael Tswett發(fā)現(xiàn)并命名的。他將植物葉子的色素通過裝填有吸附劑的柱子,各種色素以不同的速率流動后形成不同的色帶而被分開,由此得名為“色譜法”(Chromatography) 。 后來無色物質(zhì)也可利用吸附柱層析分離。 1944年出現(xiàn)紙層析。以后層析法不斷發(fā)展,相繼出現(xiàn)氣相層析、高壓液相層析、薄層層析、親和層析、凝膠層析等。 層析法是利用混合物中各組分物理化學(xué)性質(zhì)的差異(如吸附力、分子形狀及大小、分子親和力、分配系數(shù)等),使各組分在兩相(一相為固定的,稱為固定相;另一相流過固定相,稱為流動相)中的分布程度不同,從而使各組分以不同的速度移動而達(dá)到分離的目的。按層析過程的機(jī)理分類:
吸附層析:利用吸附劑表面對不同組分吸附性能的差異,達(dá)到分離鑒定的目的。 分配層析:利用不同組分在流動相和固定相之間的分配系數(shù)不同,使之分離。 離子交換層析:利用不同組分對離子交換劑親和力的不同。
凝膠層析:利用某些凝膠對于不同分子大小的組分阻滯作用的不同
紙層析法是用濾紙作為惰性支持物的分配層析法,它是利用不同的氨基酸在展層溶劑中的分配系數(shù)不同而得以分離的一種方法。惰性支持物是新華一號濾紙,其上含有很多的羥基,與水有較強(qiáng)的親和力因此把它看成是含有靜止水相的惰性支持物。水相因此稱為靜止相(固定相),有機(jī)溶劑稱為流動相。展層溶劑由兩個互不相溶的有機(jī)溶劑和水組成,它們互相混合時便分成兩相:一相是以水飽和了的有機(jī)相,另一相是以有機(jī)溶劑飽和了的水相。
分配系數(shù)(α)=溶質(zhì)在固定相的濃度(CS)/溶質(zhì)在流動相的濃度(CL)
當(dāng)用濾紙進(jìn)行分配層析時,流動相流經(jīng)支持物時與固定相之間連續(xù)抽提,使氨基酸在兩相之間不斷分配而得以分離。分配層析的原理可用一個模式解釋(英*Martin等):把濾紙看成是一個層析柱,可以分成若干層板,設(shè)層板的物質(zhì)為A、B;且A和B的分配系數(shù)(α)分別為1和1/3;又設(shè)固定相為S,流動相為L,兩相互相接觸但不相混溶。當(dāng)**層流動相中加入一定量的A、B兩項物質(zhì)后,溶質(zhì)根據(jù)各自的分配系數(shù)在**層的兩相中分配,流動相繼續(xù)在流動,此時**層固定相與新流到的流動相之間以及原來**層流動相與第二層固 定相之間進(jìn)行第二次分配,以此類推三次分配即可看出A與B**濃部分以分開,A在第二層**濃,B在第三層**濃,如果繼續(xù)抽提下去,經(jīng)過若干此后,A、兩物質(zhì)便可完全分開。顯然,分配系數(shù)越大的,則越易分開。
物質(zhì)被分離后在紙層析圖譜上的位置是用Rf值(比移值)來表示的:
Rf=原點(diǎn)到層析點(diǎn)中心的距離/原點(diǎn)到溶劑前沿的距離
在一定的條件下某種物質(zhì)的Rf值是常數(shù)。Rf值的大小與物質(zhì)的結(jié)構(gòu)、性質(zhì)、溶劑系統(tǒng);層析濾紙的質(zhì)量和層析溫度等因素有關(guān)。本實(shí)驗利用紙層析法分離氨基酸。
無色物質(zhì)的層析圖譜可用光譜法或顯色法鑒定。本實(shí)驗采用茚三酮為顯色劑。茚三酮顯色反應(yīng)受溫度、 ph、時間影響較大。如果要使結(jié)果重復(fù),必須嚴(yán)格控制上述條件。
二、實(shí)驗材料與方法
1、實(shí)驗試劑
1. 氨基酸標(biāo)準(zhǔn)液(1mg/ml)
四種氨基酸是甘氨酸、亮氨酸、脯氨酸、混合氨酸分別配置成一定濃度的溶液 2. 80%甲酸3. 0.5%茚三酮溶液 4. 氨基酸混合液 5. 正丁醇
2、實(shí)驗器材
1. 新華濾紙 2. 培養(yǎng)皿
3. 電熱鼓風(fēng)干燥箱 4. 點(diǎn)樣管及點(diǎn)樣架 5. 針、線、尺 6. 燒杯 7. 鐘罩 #p#分頁標(biāo)題#e#
3、實(shí)驗操作
(一)標(biāo)準(zhǔn)氨基酸紙上層析 1、單向上行層析
(1)氨基酸Rf值的測定 A、 濾紙:選用*產(chǎn)新華1號濾紙,28cmX28cm,在距紙邊2cm處,用鉛筆輕輕劃一條線,
于線上每隔3cm處畫一小圓圈作為點(diǎn)樣處,圈直徑不超過0.5cm。
B、 點(diǎn)樣:點(diǎn)樣要合適,樣品點(diǎn)的太濃,斑點(diǎn)易擴(kuò)散或拉長,以致分離不清,氨基酸的點(diǎn)
樣量以每種氨基酸含5—20ug為宜,將準(zhǔn)備好的濾紙懸掛在點(diǎn)樣架上,濾紙垂直桌面,用點(diǎn)樣管吸取氨基酸樣品10ug,在濾紙垂直方向輕輕碰觸點(diǎn)樣中心,這時樣品就自動流出。點(diǎn)樣的擴(kuò)散直徑控制在0.5cm之內(nèi),點(diǎn)樣過程中必須在**滴樣品干后再點(diǎn)第二滴。
C、 將點(diǎn)好的樣品的濾紙倆側(cè)比齊,用線縫好,揉成筒狀。注意縫線處的紙的倆邊不要接
觸,避免由于毛細(xì)管現(xiàn)象使溶劑沿倆邊移動特別快而造成溶劑前沿不齊,影響Rf值。
D、 酸溶劑系統(tǒng):正丁醇:80%甲酸:水=15:3:2,茚三酮2ml,溫度25*C,時間1h。注意:
使用的溶劑系統(tǒng)需新鮮配制,并要搖勻。展層溶劑每張約需25ml。
E、 顯色:待展層基本結(jié)束后,置65.C鼓風(fēng)箱中10—20min, 鼓風(fēng)保溫,濾紙上即顯出紫
紅色黃色斑點(diǎn)。
F、 Rf值的計算:用尺測量顯色斑點(diǎn)的中點(diǎn)與原點(diǎn)之間的距離和原點(diǎn)到溶劑前沿的距離,
求出此值,即得氨基酸的Rf值,計算出4種氨基酸在酸系統(tǒng)中的Rf值。
三、實(shí)驗數(shù)據(jù)與分析
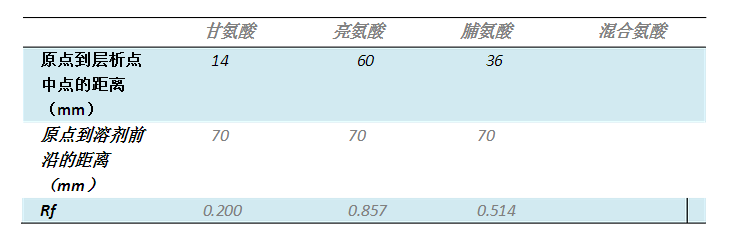
四、討論
1、注意事項
⑴.點(diǎn)樣時要避免手指或唾液等污染濾紙有效面(即展層時樣品可能達(dá)到的部分)。
⑵.點(diǎn)樣斑點(diǎn)不能太大,防止層析后氨基酸斑點(diǎn)過度擴(kuò)散和重疊,且點(diǎn)樣后吹風(fēng)溫度不宜過高,以免樣品變性(斑點(diǎn)發(fā)黃)。 ⑶.展層開始時切勿使樣品點(diǎn)浸入溶劑中。
⑷.展層劑要臨用前配制,以免發(fā)生酯化,影響層析結(jié)果。
2、思考題 ( 1)、紙層析法分離氨基酸為什么在展層時使用一種溶劑系統(tǒng),有時使用倆種溶劑系統(tǒng)?
這是根據(jù)Nernst在1891年提出的分配定律:一種溶質(zhì)在兩種給定的互不相溶的溶劑中分配時,在一定溫度下達(dá)到平衡后,溶質(zhì)在兩相中的濃度比為一常數(shù),即分配系數(shù)(Kd)。
Kd=Ca/Cb Ca和Cb是互不相溶的兩相,即A相和B相的濃度。這里的兩相可以使固相、液相和氣相。
意思就是溶質(zhì)在A和B兩種溶劑組成的混合溶劑里分配時,分配比是恒定的。 (2)、酸性溶劑系統(tǒng)對氨基酸極性基團(tuán)的解離有何影響?
酸性溶液中,有利于氨基酸的堿式電離,氨基結(jié)合質(zhì)子,整個分子帶正電荷;反之,堿性溶液中有利于羧基的酸式電離,氨基酸分子整體帶負(fù)電荷。 (3)、展層劑酸性溶劑系統(tǒng)對酸性氨基酸的Rf值有什么影響?
溶劑系統(tǒng)pH影響氨基酸電離情況,如果用有機(jī)溶劑做展層劑,那么氨基酸 電越多,溶解度越小,Rf也就越小。
